Di Alice Mannucci

Dalla fine del XX secolo sta emergendo la problematica legata alla contaminazione di suoli ed acque dai per- e polifloroalchiliche (PFAS) (Gaines, 2023). I PFAS sono delle sostanze chimiche sintetiche utilizzate nella preparazione di prodotti ad uso quotidiano (schiume antincendio, tessuti e imballaggi alimentari ecc.) (Li et al., 2020; McMahon et al., 2022; Meng et al., 2021; Reinikainen et al., 2022). L’assorbimento di PFAS può generare problemi di salute al corpo umano[1] perché persistenti, tossici ed in grado di legarsi alle proteine e alle membrane cellulari (Zhao et al., 2023; Han et al., 2023) (Figura 1).
L’esposizione ai PFAS può avvenire tramite inalazione, ingestione orale e contatto cutaneo (ATSDR, 2021; U.S. EPA, 2023). Pertanto il consumo di acqua potabile e cibo contaminati sono riconosciute come fonti primarie di accumulo di PFAS[2] nel corpo umano. Tuttavia è ancora in atto la ricerca per stabilire un collegamento definitivo tra l’esposizione a specifici PFAS e gli effetti sulla salute, soprattutto perché i composti PFAS sono stati identificati solo di recente (Wee e Aris, 2023; U.S. HHS, 2016).
A causa della idrofobicità i PFAS sono stati collocati nella lista degli inquinanti organici persistenti (Persistent Organic Pollutants, POP). I POP sono composti con proprietà tossiche per gli organismi viventi e che risultano molto resistenti alla decomposizione naturale. Questo li rende persistenti anche ai processi fisiologici che avvengono all’interno degli organismi viventi, per questo sono stati rilevati PFAS in diversi organi umani (polmoni, nel cervello, nel fegato, nelle ossa e nei reni) (Koelmel et al., 2023; Lin et al., 2023; Pèrez et al., 2013; Zhao et al., 2023).
[1] U.S. HHS, 2016: https://www.hhs.gov/sites/default/files/2016-sustainability-plan.pdf
[2] U.S. EPA, 2023: https://www.epa.gov/system/files/documents/2022-08/fy-2023-2024-ocfo-npg-overview.pdf
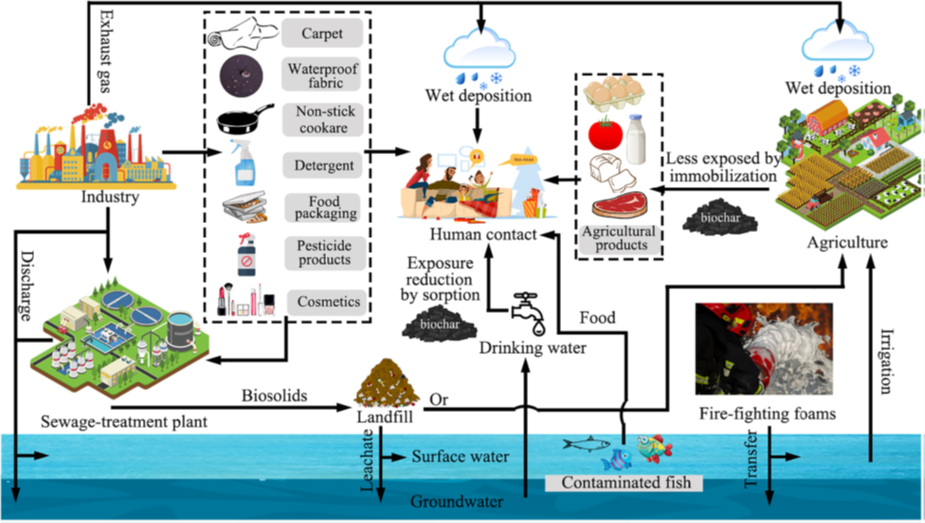
Figura 1- Fonti antropiche di PFAS e il possibile uso del biochar per la rimozione di questi dagli ambienti acquatici e suoli. (Immagine ripresa da Liang et al. 2024)
Normativa PFAS
Nel 2001, per la prima volta un sottogruppo di sostanze appartenenti ai PFAS, i PFOS, sono state riconosciute come nocive all’ambiente e all’uomo. Per questo motivo la loro produzione deve essere limitata. I PFOS e i suoi Sali, figurano nell’ allegato B della Convenzione di Stoccolma[1] come POP. La convenzione, sebbene siglata nel 2001, è entrata in vigore il 17 maggio 2004 ed è stata sottoscritta da 181 paesi. Secondo quanto sancito dalla convenzione nonostante esistano delle sostanze alternative ai PFOS questi possono, in alcuni casi, essere utilizzati[2].
Nel 2007, l’Unione Europea ha provveduto, con il piano di attuazione “Community Implementation Plan”, aggiornato nel 2014, a perseguire quanto stato sancito dalla Convenzione di Stoccolma del 2001. Con questo piano la comunità europea si impegna a individuare strategie utili per limitare la diffusione in ambiente di queste sostanze inquinanti. L’Italia, ad ora è l’unico stato firmatario europeo ad aver disatteso la Convenzione del 2001.
L’impegno della comunità europea è proseguito nel 2010 con la Raccomandazione 161 (2010/161/UE)[3]. Il documento si impegna i paesi comunitari al controllo nel territorio e negli alimenti delle sostanze perfluoroalchiliche e dei loro precursori, perfluoroottanosulfonamide (PFOSA), l’N-etilperfluoroottanosulfonamidetanolo (N-EtFOSE) e l’ 8:2 fluorotelomero degli alcool (FOET).
In fine il 4 luglio 2020 l’Unione Europea ha provveduto a vietare la produzione o l’utilizzo dei PFOA e i suoi Sali.
Negli Stati Uniti l’agenzia statunitense per la salvaguardia ambientale, EPA (Agenzia per la Protezione Ambientale), ha fissato un limite di 70 ppt per PFOA e PFOS nell’acqua potabile [7]. Tuttavia, il 10 aprile 2024, l’USEPA ha dichiarato che circa 83-105 milioni di persone negli USA attingono a riserve di acqua in cui i livelli di PFAS sono ben superiori. Una situazione simile si trova in Canada dove più di 100 siti hanno riportato livelli elevati di PFAS.
[1] http://www.pops.int/TheConvention/ThePOPs/AllPOPs/tabid/2509/Default.aspx#LiveContent[PFOS-PFOSF]
[2]http://chm.pops.int/Implementation/Alternatives/AlternativestoPOPs/ChemicalslistedinAnnexB/Perfluorooctanesulfonicacid and perfluorooctane/tabid/5869/Default.aspx
[3] https://eur-lex.europa.eu/legal-content/IT/TXT/PDF/?uri=CELEX:32010H0161
I PFAS
I PFAS sono una classe di composti chimici di sintesi appartenenti sia alla categoria degli Emerging Contaminants (EC)[1]. Sono costituiti da una catena alchilica di lunghezza variabile completamente o parzialmente fluorurata, formata da 4 a 16 atomi di carbonio. Possono presentare o un gruppo funzionale carbossilico o un gruppo solfonico[2] (Figura 2). I PFAS vengono definiti anche “Forever Chimicals“, un vasto gruppo di sostanze con un’elevata stabilità termica, chimica e biologica che li rende scarsamente solubili in acqua e quindi resistenti ai naturali di degradazione causando fenomeni di bioaccumulo e biomagnificazione (Naidu et al., 2020; Oh et al., 2024; Simon et al., 2019).
I PFAS possono essere suddivisi in tre categorie principali, sulla base di criteri strutturali: PFAS a catena lunga, PFAS a catena corta e i derivati dei PFAS. I PFOS e PFOA sono considerati i contaminanti perfluoroalchilici più rappresentativi tra i PFAS, proprio perché sono anche i prodotti di degradazione finale della maggior parte dei composti fluorurati (Raccomandazione UE 161/2010). Nonostante le restrizioni all’utilizzo e alla produzione dei PFAS a catena lunga, quelli a catena corta possono essere attualmente utilizzati come loro sostituti. Anche i PFTE non presentano attualmente restrizioni di produzione.
I PFAS a catena lunga
I PFAS a catena lunga sono il primo tipo di PFAS ad essere stati prodotti. alla categoria appartengono i derivati di due composti base: PFOA (acido perfluoroottanoico) e PFOS (acido perfluoroottansolfonico).
In particolare il PFOA è costituito da una catena alchilica completamente fluorurata e da un gruppo terminale carbossilico. Questo composto si trova in forma dissociata se posto in una acquosa acida (pH4). In queste condizioni, infatti, la catena perfluoroalchilica resta sulla superficie, a livello dell’interfaccia aria/acqua, mentre il gruppo carbossilico rimane ruotato verso l’acqua[3] (US EPA, 2005).
Il PFOA, sotto forma di acido dissociato ha tensione di vapore molto bassa che lo rende difficile da assorbire. Conseguentemente tende ad accumularsi nelle acque superficiali.
Il PFOS, come il PFOA, è costituito da una catena alchilica completamente fluorurata ma contiene un gruppo terminale solfonico (Figura 2). Si utilizza solitamente sotto forma di sale di ammonio, sodio o potassio, oppure in forma polimerizzata. Anche il PFOS si trova in forma dissociata in acque con pH compresi tra 3 e 8. La produzione del PFOS è principalmente industriale. Ad oggi il PFOS e i suoi derivati sono considerati i contaminanti più diffuso nei prodotti alimentari e in concentrazioni più alte[4].
[1] Gli ECs sono materiali chimici, sintetici o naturali, normalmente non rilevabili nell’ambiente, ma capaci di diffondersi al suo interno causando effetti dannosi ad esso e/o alla salute dell’uomo; https://www.sciencedirect.com/topics/earth-and-planetarysciences/emerging-contaminant
[2] Progetto PFAS Uda “Bevi che ti PFASsi!” prodotto dall’ITA Trentin di Lonigo nell’anno scolastico 2018-2019
[3] US EPA 2005: “Draft risk assessment of the potential human health effects associated with exposure to perfluorooctanoic acid and Its salts (PFOA)” 1-117
[4] http://amsdottorato.unibo.it/6424/1/Devicienti_Chiara_tesi.pdf
I PFAS
I PFAS sono una classe di composti chimici di sintesi appartenenti sia alla categoria degli Emerging Contaminants (EC)[1]. Sono costituiti da una catena alchilica di lunghezza variabile completamente o parzialmente fluorurata, formata da 4 a 16 atomi di carbonio. Possono presentare o un gruppo funzionale carbossilico o un gruppo solfonico[2] (Figura 2). I PFAS vengono definiti anche “Forever Chimicals“, un vasto gruppo di sostanze con un’elevata stabilità termica, chimica e biologica che li rende scarsamente solubili in acqua e quindi resistenti ai naturali di degradazione causando fenomeni di bioaccumulo e biomagnificazione (Naidu et al., 2020; Oh et al., 2024; Simon et al., 2019).
I PFAS possono essere suddivisi in tre categorie principali, sulla base di criteri strutturali: PFAS a catena lunga, PFAS a catena corta e i derivati dei PFAS. I PFOS e PFOA sono considerati i contaminanti perfluoroalchilici più rappresentativi tra i PFAS, proprio perché sono anche i prodotti di degradazione finale della maggior parte dei composti fluorurati (Raccomandazione UE 161/2010). Nonostante le restrizioni all’utilizzo e alla produzione dei PFAS a catena lunga, quelli a catena corta possono essere attualmente utilizzati come loro sostituti. Anche i PFTE non presentano attualmente restrizioni di produzione.
I PFAS a catena lunga
I PFAS a catena lunga sono il primo tipo di PFAS ad essere stati prodotti. alla categoria appartengono i derivati di due composti base: PFOA (acido perfluoroottanoico) e PFOS (acido perfluoroottansolfonico).
In particolare il PFOA è costituito da una catena alchilica completamente fluorurata e da un gruppo terminale carbossilico. Questo composto si trova in forma dissociata se posto in una acquosa acida (pH4). In queste condizioni, infatti, la catena perfluoroalchilica resta sulla superficie, a livello dell’interfaccia aria/acqua, mentre il gruppo carbossilico rimane ruotato verso l’acqua[3] (US EPA, 2005).
Il PFOA, sotto forma di acido dissociato ha tensione di vapore molto bassa che lo rende difficile da assorbire. Conseguentemente tende ad accumularsi nelle acque superficiali.
Il PFOS, come il PFOA, è costituito da una catena alchilica completamente fluorurata ma contiene un gruppo terminale solfonico (Figura 2). Si utilizza solitamente sotto forma di sale di ammonio, sodio o potassio, oppure in forma polimerizzata. Anche il PFOS si trova in forma dissociata in acque con pH compresi tra 3 e 8. La produzione del PFOS è principalmente industriale. Ad oggi il PFOS e i suoi derivati sono considerati i contaminanti più diffuso nei prodotti alimentari e in concentrazioni più alte[4].
[1] Gli ECs sono materiali chimici, sintetici o naturali, normalmente non rilevabili nell’ambiente, ma capaci di diffondersi al suo interno causando effetti dannosi ad esso e/o alla salute dell’uomo; https://www.sciencedirect.com/topics/earth-and-planetarysciences/emerging-contaminant
[2] Progetto PFAS Uda “Bevi che ti PFASsi!” prodotto dall’ITA Trentin di Lonigo nell’anno scolastico 2018-2019
[3] US EPA 2005: “Draft risk assessment of the potential human health effects associated with exposure to perfluorooctanoic acid and Its salts (PFOA)” 1-117
[4] http://amsdottorato.unibo.it/6424/1/Devicienti_Chiara_tesi.pdf
I PFAS
I PFAS sono una classe di composti chimici di sintesi appartenenti sia alla categoria degli Emerging Contaminants (EC)[1]. Sono costituiti da una catena alchilica di lunghezza variabile completamente o parzialmente fluorurata, formata da 4 a 16 atomi di carbonio. Possono presentare o un gruppo funzionale carbossilico o un gruppo solfonico[2] (Figura 2). I PFAS vengono definiti anche “Forever Chimicals“, un vasto gruppo di sostanze con un’elevata stabilità termica, chimica e biologica che li rende scarsamente solubili in acqua e quindi resistenti ai naturali di degradazione causando fenomeni di bioaccumulo e biomagnificazione (Naidu et al., 2020; Oh et al., 2024; Simon et al., 2019).
I PFAS possono essere suddivisi in tre categorie principali, sulla base di criteri strutturali: PFAS a catena lunga, PFAS a catena corta e i derivati dei PFAS. I PFOS e PFOA sono considerati i contaminanti perfluoroalchilici più rappresentativi tra i PFAS, proprio perché sono anche i prodotti di degradazione finale della maggior parte dei composti fluorurati (Raccomandazione UE 161/2010). Nonostante le restrizioni all’utilizzo e alla produzione dei PFAS a catena lunga, quelli a catena corta possono essere attualmente utilizzati come loro sostituti. Anche i PFTE non presentano attualmente restrizioni di produzione.
I PFAS a catena lunga
I PFAS a catena lunga sono il primo tipo di PFAS ad essere stati prodotti. alla categoria appartengono i derivati di due composti base: PFOA (acido perfluoroottanoico) e PFOS (acido perfluoroottansolfonico).
In particolare il PFOA è costituito da una catena alchilica completamente fluorurata e da un gruppo terminale carbossilico. Questo composto si trova in forma dissociata se posto in una acquosa acida (pH4). In queste condizioni, infatti, la catena perfluoroalchilica resta sulla superficie, a livello dell’interfaccia aria/acqua, mentre il gruppo carbossilico rimane ruotato verso l’acqua[3] (US EPA, 2005).
Il PFOA, sotto forma di acido dissociato ha tensione di vapore molto bassa che lo rende difficile da assorbire. Conseguentemente tende ad accumularsi nelle acque superficiali.
Il PFOS, come il PFOA, è costituito da una catena alchilica completamente fluorurata ma contiene un gruppo terminale solfonico (Figura 2). Si utilizza solitamente sotto forma di sale di ammonio, sodio o potassio, oppure in forma polimerizzata. Anche il PFOS si trova in forma dissociata in acque con pH compresi tra 3 e 8. La produzione del PFOS è principalmente industriale. Ad oggi il PFOS e i suoi derivati sono considerati i contaminanti più diffuso nei prodotti alimentari e in concentrazioni più alte[4].
[1] Gli ECs sono materiali chimici, sintetici o naturali, normalmente non rilevabili nell’ambiente, ma capaci di diffondersi al suo interno causando effetti dannosi ad esso e/o alla salute dell’uomo; https://www.sciencedirect.com/topics/earth-and-planetarysciences/emerging-contaminant
[2] Progetto PFAS Uda “Bevi che ti PFASsi!” prodotto dall’ITA Trentin di Lonigo nell’anno scolastico 2018-2019
[3] US EPA 2005: “Draft risk assessment of the potential human health effects associated with exposure to perfluorooctanoic acid and Its salts (PFOA)” 1-117
[4] http://amsdottorato.unibo.it/6424/1/Devicienti_Chiara_tesi.pdf
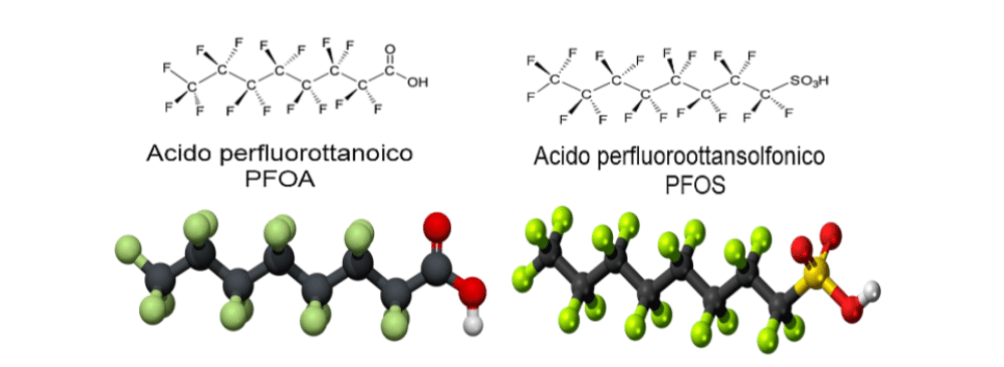
Figura 2 – Lungo la catena alchilica, a lunghezza, da 4 a 16 atomi di carbonio, si possono trovare o gruppi funzionali carbossilici o solfonici. Immagine ripresa da: https://bioeticaliceoscarpa.altervista.org/documenti/1920_PFAS_Classi5.pdf
I PFAS a catena corta
I PFAS a catena sono costituiti da catene carboniose da 4-6 atomi di carbonio. I principali PFAS a catena corta includono il PFBA (acido perfluorobutanoico, C4HF7O2), il PFHxA (acido perfluoroesanoico, C6HF11O2) e il PFBS (acido perfluorobutansulfonico, C4HF9O3S) (Zanon, et al. 2017). Tali PFAS hanno proprietà simili a PFOS e PFOA, ma sono caratterizzati da una minore resistenza alle alte temperature e minori proprietà repellenti ad acqua e olio.
I Derivati
Tra i derivati dei PFAS il più importante è il PTFE (Politetrafluoroetilene), commercialmente conosciuto come Teflon. Ha struttura simile ai PFAS, ma è caratterizzato dalla mancanza dei gruppi funzionali terminali. Ciò ne influenza l’acidità e ne determina una maggiore inerzia chimica. E’ caratterizzato dalla completa insolubilità in qualsiasi solvente organico e in acqua. Ha inoltre ottime qualità dielettriche, resistenza al fuoco (non propaga la fiamma), scorrevolezza superficiale (coefficiente d’attrito più basso tra i prodotti industriali), proprietà antiaderenti.
Soluzioni all’inquinamento da PFAS
Per porre rimedio all’inquinamento da PFAS sono state studiate diverse tecniche relative ai diversi contesti di corpi idrici o suoli inquinati.
Nel primo caso, viene prediletta la tecnica di filtrazione con carboni attivi, ma altri metodi utilizzati sono: la chiariflocculazione, i processi a membrana e i processi di ossidazione ad opera di agenti ossidanti.
Qualora invece sia il suolo ad essere inquinato, le procedure prevedono l’applicazione diretta di una fonte di calore. Questo sistema sfrutta la vaporizzazione delle sostanze chimiche come conseguenza dell’applicazione di alte temperature (400° C circa) (Husek et al., 2024). Altri studi stanno ipotizzando il ricorso alla fitodepurazione (Evangelou e Robinson, 2022) per limitare i fenomeni di lisciviazione ed erosione e dunque ridurre la mobilità dei PFAS. Tuttavia, questa ipotesi non rimane risolutiva sul problema principale dato dai PFAS, ossia la loro persistenza (Gobelius et al., 2017; Lyu et al., 2022).
Recentemente tra le sostanze carboniose testate per l’adsorbimento di PFAS presenti in ambe due i contesti, soluzioni acquose e suolo, è stato individuato il biochar, carbone vegetale ottenuto dalla degradazione termochimica di biomasse (Mayakaduwage et al., 2022; Liang et al., 2024).
Il biochar come possibile soluzione
Il biochar, noto soprattutto nei settori agro-forestali come ammendante, sta emergendo anche in altri settori per le sue molteplici potenzialità (Gagliano et al., 2020; Liu et al., 2024). Diversi studi hanno dimostrato che questo materiale presenta una buona capacità di adsorbimento dovuta sia alla struttura porosa che alla presenza di gruppi funzionali, quali idrossilici, carbossilici e carbonilici in grado di interagire con i PFAS (Bui et al.,2024) (Tabella 1). Per questo diversi autori sostengono che il biochar attivato può essere la soluzione al problema dell’inquinamento da PFAS.
Inoltre, il biochar può essere sottoposto a trattamenti d’attivazione, che lo rendono ancora più prestante nelle sue capacità adsorbenti. Intervenire sulle caratteristiche fisico-chimiche significa, ad esempio, aumentare la superficie specifica e la porosità incrementando i meccanismi di assorbimento fisico e le interazioni idrofobiche (Wang et al., 2023; Hassan et al., 2025). Quest’ultime, in particolare, secondo Teng et al. (2024) sono il meccanismo principale che controlla l’adsorbimento di PFAS. Tuttavia, queste interazioni risultano strettamente correlate alla lunghezza della catena dei PFAS. All’aumentare della lunghezza della catena aumenta l’idrofobicità della specie PFAS, perché la lunghezza della catena è data da un numero maggiore di legami C–F (Krahn et al., 2023). Questo rende il biochar potenzialmente prestante nell’adsorbimento dei PFAS a catena lunga, ma limitato nella rimozione di quelli a catena corta (Liu et al., 2020). Per rendere efficiente il biochar anche rispetto a questi è necessario ricorrere a strategie di attivazione in grado di aggiungere o potenziale le proprietà catalitiche necessarie.
Il biochar dunque si presenta come una soluzione promettente per mitigare i rischi associati alla contaminazione da PFAS nei terreni e nelle acque contaminate (Wang et al., 2023a). Tuttavia, sono necessarie ulteriori ricerche e sforzi perché sebbene siano molteplici gli articoli al riguardo, questi non sono ancora sufficiente a causa dell’infinita possibilità di miscele in cui i PFAS possono presentarsi in natura (Hassan et al., 2025).
| Tipi di biochar | Suoli | TOC (%) | (w/W) % | Riduzione dei PFAS (%) | Referenze | |||
| PFOS | PFOA | PFHxS | PFHxA | |||||
| Pine biochar | Loamy sand soil | – | 5 | 20.1 | 41.6 | 28.3 | 19.3 | (Askeland et al., 2020) |
| Sandy clay loam | – | 5 | 42.7 | 58.9 | 26.8 | 45.4 | ||
| Waste timber biochar | Moraine soil | 1.6 | 1 | 93 | 72 | 81 | 61 | (Sørmo et al., 2021) |
| 1.6 | 5 | 100 | 100 | 100 | 100 | |||
| 34.2 | 1 | 59 | 21 | 17 | 22 | |||
| 34.2 | 5 | 78 | 51 | 59 | 38 | |||
| Shredded timber waste biochar | Eluvial and illuvial mineral horizons | 1.6 | 20 | 86 | 70 | 72 | 31 | (Silvani et al., 2019) |
| Forest wood waste biochar | Sandy loam soil | – | 2 | 9.8 | 22.1 | 32.5 | 50.9 | (Zhang and Liang, 2022a) |
| Forest wood waste biochar | Sandy loam texture | 1.6 | 2 | 24.5 | 42.8 | 43.5 | 64.6 | (Zhang and Liang, 2022b) |
| Sludge biochars | Sandy soil | 0.57 | 1 | 92–99 | 80–85 | 75–79 | 35–40 | (Sørmo et al., 2024) |
Tabella 1- Elenco di studi sulle performance adsorbenti dei biochar in suoli inquinati da PFAS. (Liang et al. 2024)
Il biochar
Il biochar è un materiale organico composto principalmente di carbonio. Talvolta viene definito “Carbone Vegetale” perché ottenuto da processi di degradazione termochimica di varie tipologie di biomasse. Queste possono includere scarti agricoli e forestali, rifiuti urbani, industriali e derivati animali (letame e pollina) (Chen et al., 2024, 2023; Li et al., 2024a; Masud et al., 2023). Il biochar ha suscitato l’interesse della comunità scientifica sia per le sue caratteristiche fisico-chimiche come la struttura porosa, l’elevata superficie specifica e affinità ionica, sia per la possibilità di intervenire su queste scegliendo le materie prime e il processo produttivo da utilizzare. A concorrere con gli attributi fisico-chimici si aggiunge la stabilità del carbone recalcitrante di cui è composto (Wen et al., 2023). Il biochar infatti può essere descritto come una lega carboniosa, il cui carbonio si trova nella forma stabile, inerte. In fine, il biochar è un prodotto bio-base, oltre che una Carbon-Dioxide Rimoval Strategy (Van Nguyen et al., 2022). La trasformazione delle biomasse in carbonio recalcitrante (bioochar) consente di sottrarre all’ambiente, la CO2 altrimenti prodotta dai naturali processi di degradazione di queste. Il potenziale C-sink del biochar se valutato e certificato può essere anche utilizzato per la creazione dei carbon-credits.
Le proprietà fisico-chimiche del biochar
Biochar è un termine generico utilizzato per indicare quei composti carboniosi ottenuti dalla degradazione termochimica di biomasse di vario tipo. Per questo motivo essi presentano differenze nelle caratteristiche fisiche e chimiche. Conseguentemente ogni biochar ha un potenziale assorbente differente nei confronti dei composti PFAS (Liang et al. 2024).
Caratteristiche fisiche
Il biochar, derivando della degradazione termochimica di biomasse, presenta una distribuzione granulometrica dipendente dalla composizione della biomassa originaria e dalle specifiche del processo termochimico utilizzato. Per questo motivo non tutti i biochar presentano una medesima distribuzione delle percentuali granulometriche. In generale la frazione cineritica aumenta all’aumentare delle temperature. Per tale motivo, questa risulta presente in percentuale maggiore nei biochar derivanti da piro-gassificazioni o gassificazione (cit). Similmente la dimensione e la percentuale della componente porosa è determinata sia dalla struttura della biomassa sia del temperature nel reattore. In questo caso, però si aggiunge anche il fattore permanenza nel reattore. Infatti superata la soglia di permanenza di 2 ore (a T= 500–900°C), i pori si riducono a causa del contatto con i gas prodotti dai processi termochimici (Zhang et al., 2015; Lee et al., 2013; Bandosz et al., 2006). Conseguentemente la densità apparente e la superficie specifica variano in funzione di questi parametri. La superficie specifica, tendenzialmente compresa intorno ai valori 360-500 m2/g (Chiaramonti, 2019), è una delle caratteristiche più influenti sulle potenzialità adsorbenti del biochar. Determinata dal tipo di biomassa impiegata e dal processo pirolitico, essa consente dunque la formazione di siti attivi e conseguentemente la possibilità di fissare l’inquinante sulla superficie del biochar.
Caratteristiche chimiche
Come le caratteristiche fisiche anche quelle chimiche sono determinate dai fattori: composizione della biomassa di partenza, temperatura e tempo di permanenza nel reattore. Nel considerare il biochar come composto carbonioso adsorbente fattori determinanti sono il pH, la superficie specifica, tipologie di gruppi funzionali, presenza di specie ioniche (CEC) e rapporto ossigeno- carbonio (O/C). Tuttavia, le performance adsorbenti del biochar sono determinate anche dalle specifiche chimiche delle specie adsorbite.
In particolare, per la rimozione dei PFAS risultano fondamentali la presenza di alcuni tipi di gruppi funzionali, rapporti O/C bassi ed elevati CEC.
Il rapporto O/C viene considerato indice del grado di carbonizzazione, perché all’aumentare delle temperature l’ossigeno passa in stato gassoso (CO2, CO, H2O) e quindi il rapporto risulta direttamente proporzionale alle temperature impiegate nel reattore. Per questo motivo, un rapporto basso O/C è tipico di biochar derivanti da piro-gassificazione o gassificazione. il grado di carbonizzazione è determinate anche sul grado di aromaticità del composto carbonioso. All’aumentare delle temperature, in particolare superati i 550° C si nota una riduzione dei gruppi funzionali ossidrili e idrossili a favore di quelli aromatici. Come diretta conseguenza della maggiore aromaticità, si osserva una riduzione della polarità superficiale ed aumento delle interazioni idrofobiche tra i gruppi funzionali aromatici e i PFAS. Mentre la presenza di specie ioniche sulla superficie del biochar contribuisce all’adsorbimento dei PFAS fornendo siti di scambio ionico. Secondo Nasrollahpour et al. (2025) i biochar con CEC più alti sono più efficaci, in particolare per i PFAS cationici o zwitterionici, a causa delle maggiori interazioni elettrostatiche. Nasrollahpour et al. (2025) riportano che ad influenzare i risultati concorrono anche fattori come la presenza di ioni in competizione e il pH.
Biochar e i PFAS
Fattori determinanti che rendono il biochar un materiale adsorbente sono: l’elevata superficie specifica, la struttura porosa, la capacità di scambio ionico e la presenza di diversi gruppi funzionali (Krebsbach et al., 2023a; Park et al., 2020; Saeidi et al., 2020).
La superficie specifica e la porosità sono influenzate dalla materia prima e dal processo di produzione. Esse rendono possibile fenomeni di adsorbimento fisico. Contaminanti come le molecole organiche (Idrocarburi Aromatici Policiclici (IPA) e i pesticidi) vengono, ad esempio, intrappolate nei micropori e fissati dalle forze di Van Der Waals (Nasrollahpour et al., 2025). La presenza di gruppi funzionali, quali idrossile (-OH), carbossile (-COOH) e ammina (-NH2), presenti sulla superficie del biochar, invece consentono di fermare legami chimici (ioni, ad idrogeno e covalenti forti) con le molecole contaminanti. In questi casi si tratta di adsorbimento chimico.
Tuttavia l’efficienza del processo di adsorbimento è influenzata anche dal pH, dalla forza ionica, dalla temperatura e dalla presenza di contaminanti concorrenti (Nasrollahpour et al., 2025).
La Porosità
Accanto alle caratteristiche chimiche, anche la dimensione delle particelle di biochar è risulta essere parametro critico nella performance di assorbimento dei PFAS. Secondo quanto riportato in letteratura le particelle più piccole, in genere, mostrano una capacità adsorbente più elevata. Ad un indice di micro-porosità elevato corrisponde anche una superficie specifica maggiore e un numero maggiore di siti attivi a disposizione. Lo studio di Hassan et al. (2020) ha infatti riportato un miglioramento delle prestazioni adsorbenti nei biochar aventi dimensioni dei pori medie di circa 0,5 mm rispetto a quelli aventi dimensioni maggiori (Figura 3). La differenza nelle prestazioni può essere attribuita oltre che ad una maggiore superficie specifica e disponibilità siti attivi, anche per la riduzione del fenomeno di diffusione intraparticellare (Hassan et al., 2020; Xiao et al., 2017). Nonostante questi vantaggi, la microporosità, consistenti in dimensioni medie ≤ 0,5mm possono indurre ad altri tipi di difficoltà. Ad esempio nelle procedure di rigenerazione dei biochar. Pertanto, è necessario individuare la dimensione ottimale dei pori che dia modo di ottenere le prestazioni di adsorbimento desiderate e consenta il recupero del materiale (Xiao et al., 2017).
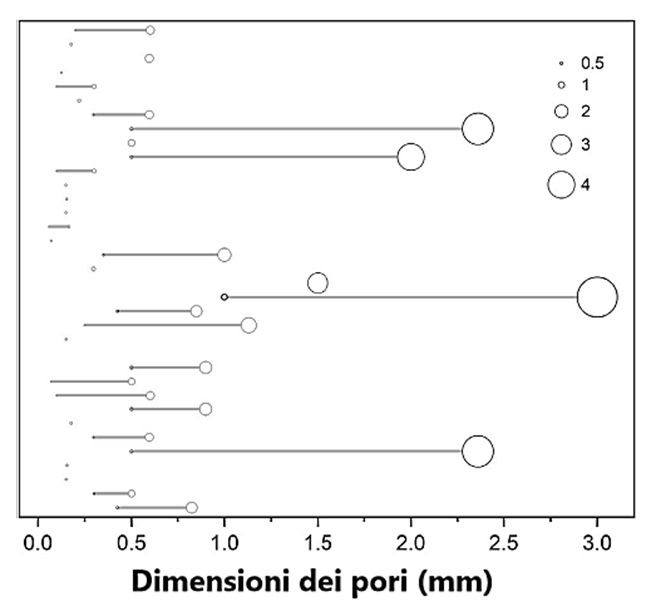
Figura 3- Dimensioni delle porosità dei biochar riportate in letteratura nelle prove di adsorbimento di PFAS. (Nasrollahpour et al., 2025)
I gruppi funzionali
Nelle reazioni di complessazione svolgono un ruolo fondamentale i gruppi funzionali presenti sulla superficie del biochar. La tipologia e la quantità di gruppi funzionali varia in funzione della temperatura raggiunta durante il processo pirolitico (Keiluweit et al., 2010). I biochar derivanti da processi a temperature basse o intermedie (300–450° C), presentano concentrazioni e varietà di gruppi funzionali decisamente superiori rispetto ai biochar ottenuti da processi in cui le temperature raggiunte superano 750° C (Janu et al., 2021). Questo è evidente dallo spettro FTIR ripostato di seguito (Figura 3). Questo confronta i gruppi funzionali relativi a due biochar ottenuti da processi pirolitici diversi. Il biochar, indicato con BC5, è stato ottenuto da pirolisi lenta, con temperature massime ≈ 550° C, mentre il BC7 da un processo di pirogassificazione con picco termico di 850°C (Animali et al., 2025).
Lo spettro del primo (BC5) evidenzia la presenza di: C-H aromatici (3000-3100 [cm-1]), C-H alifatici (2800-300 [cm-1]), gruppi ossigenati C=O (carbonil/carbossilico) (1690 [cm-1]), e il gruppo C=C delle catene aromatiche e/o olefiniche, visibili a 1564 cm-1 e 1432 cm-1, dovuti alle vibrazioni C=C nell’anello aromatico e/o allo stretching alifatico CH2 e CH3. Mentre lo spettro del BC7 presenta un picco importante in corrispondenza delle bande dei C=C aromatici (1565 -1430 [cm-1]), altri due picchi nelle bande riconducibili ai CH3 alifatici (1385-1370 [cm-1]) e alle vibrazioni out of plane del gruppo C-H (880-750 [cm-1]) (Animali et al. 2025)
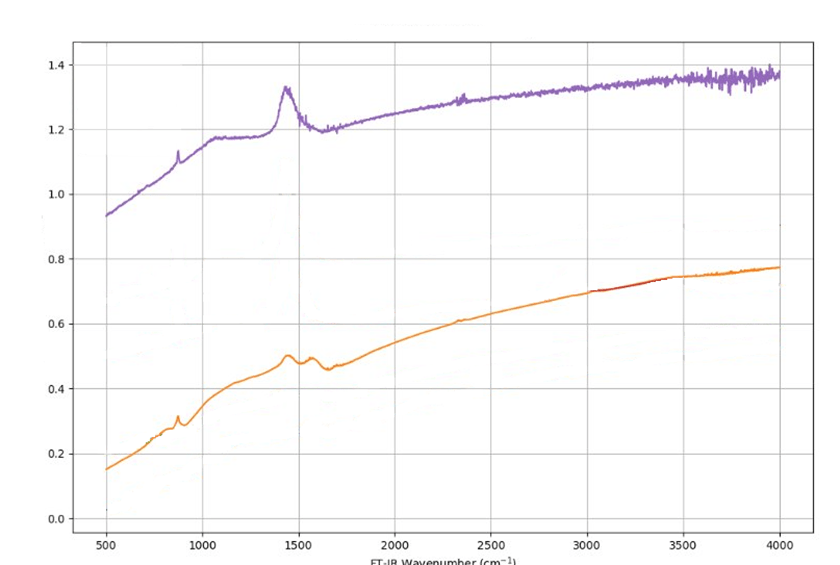
Figura 3 – Spettri FT-IR appartenenti a 2 biochar derivanti da processi termochimici differenti: il BC5 (arancione) da pirolisi lenta Tmax. =550° C e il BC7 (viola) da pirogassificazione Tmax. 850° C.
Un’analisi degli spettri FTIR del biochar prima e dopo l’adsorbimento del PFAS, rivela che i gruppi funzionali esteri carbossilici possono contribuire in modo significativo all’interazione elettrostatica e all’adsorbimento complesso delle sostanze PFAS (Wahab et al., 2010; Zhang et al., 2021). L’atomo di fluoro (F-), presente come radicale nelle molecole dei PFAS, interagisce con lo ione idrossile (OH-), presente sulla superficie del biochar, creando un legame ad idrogeno.
Il pH
Il fattore pH è determinante sulle performance di adsorbimento dei biochar. Questo determina la carica superficiale del biochar (pHpzc[1]). Se questa è carica positivamente consente la formazione di complessi con i PFAS caricati negativamente (Hassan et al., 2020; Lyu et al., 2022). Se il pH del biochar è negativo, i gruppi funzionali sulla superficie del biochar vengono facilmente protonati acquisendo una carica positiva. Questo processo di protonazione facilita la rimozione di PFOS attraverso reazioni di scambio ionico e interazioni elettrostatiche (Hassan et al., 2020). All’aumentare del pH, aumenta il processo di deprotonazione dei gruppi funzionali (Liu et al. 2023b). Tuttavia l’aumento del pH innesca anche una reazione di repulsione elettrostatica dei PFOA e del PFBA anionici e questo porta ad una diminuzione della capacità adsorbente. Il valore ottimale di pH è di 4,3 (Kundu et al., 2021) (Figura 2).
È importante ricordare che, il pH del biochar è influenzato anche della fase liquida con cui esso viene in contatto e che il pH non determina solo la carica superficiale del biochar, ma le reazioni di ionizzazione dei soluti e la generazione di altre sostanze (Gao et al., 2017; Zhang et al., 2021).
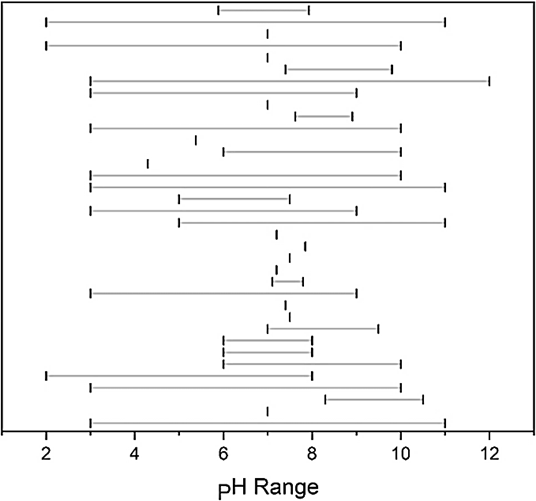
Figura 2- intervalli di pH individuati dai diversi studi che hanno indagato sulle capacità del biochar di rimuovere i PFAS. (Nasrollahpour et al., 2025)
[1] pHpzc : Punto di carica zero, la superficie del biochar è neutra netta. Al di sopra del pHpzc, la superficie acquisisce carica netta negativa, mentre al di sotto si osserva una carica netta positiva (Fabregat-Palau et al., 2022).
Processi di attivazione
Le procedure di attivazione dei biochar vengono eseguite con lo scopo di migliorare le performance di rimozione dei PFAS. A tale proposito, queste puntano a potenziare le caratteristiche chimico-fisiche dei biochar così da incrementare le interazioni elettrostatiche, idrofobiche e di Van der Waals. Dunque le tecniche di attivazione agiscono sulla chimica di superficie, sulla superficie specifica e il numero e tipologia di gruppi funzionali. La Tabella 2 illustra i diversi approcci sperimentati sui biochar in riferimento agli inquinanti PFAS. Queste possono consistere in approcci fisici, chimici e biologici. Tuttavia quelle che ad ora più efficienti prevedono un trattamento chimico (Chen et al., 2022; Lu et al., 2022). Circa metà degli studi infatti ha testato l’attivazione dei biochar con KOH e ZVI.
Nel primo caso si tratta di biochar impregnati con nanoparticelle funzionali (nanoparticelle di ferro (nZVI), grafene, nanotubi di carbonio e ossidi metallici come ZnS e Fe3O4). Queste consentono di migliorarne le proprietà del biochar agendo sulla reattività di quest’ultimo. Ad esempio, il biochar modificato con nZVI può indurre reazioni redox, facilitando la scomposizione delle molecole di PFAS. Contemporaneamente, l’elevata superficie specifica e la reattività delle nanoparticelle agiscono limitando le potenziali ostruzioni della struttura porosa del biochar. Gli studi rivelano che il biochar attivato in questo modo può raggiungere un tasso di rimozione del 99,9% di PFOA [2]alte temperature entro 6 ore (Nasrollahpour et al., 2025). Questo risultato è stato attribuito alla formazione di aggregati di particelle di nZVI durante il processo termico. I quali faciliterebbero la degradazione dei PFAS.
La variabilità composizionale e strutturale dei biochar, implica però specifici adattamenti del trattamento (Yang et al., 2022). In aggiunta, nonostante i risultati promettenti, deve essere considerato l’aspetto di pericolo ambientale; è possibile, infatti, che avvenga il rilascio da parte del biochar di nanoparticelle, creando problematiche ambientali importanti.
[2] Lo studio ha osservato l’effetto adsorbente del biochar potenziato con nanoparticelle nZVI in condizioni di elevate temperature ed un esposizione di 6 ore.
Biochar magnetizzato
L’attivazione tramite ferro, procedura meglio nota come “magnetizzazione”, comporta l’incorporazione di materiali magnetici, tipicamente ossidi di ferro (come Fe3O4), tramite metodi come pirolisi o co-precipitazione. Questi consentono di separare facilmente il biochar dalle particelle inquinanti ricorrendo a semplici magneti. Il biochar magnetico è infatti interessante per le procedure di trattamento delle acque reflue (Thines et al., 2017).
Il biochar magnetizzato risulta efficiente anche nell’adsorbimento dei PFAS perché implementa le interazioni elettrostatiche e il chemisorbimento (Hassan et al., 2020). Il fenomeno principale è la deprotonazione dei gruppi funzionali, che favorisce a sua volta, la formazione di legami a idrogeno con i PFAS (Fang et al., 2014; Liu et al., 2023b). In particolare, secondo Gagliano et al. (2020) con quelli a catena corta. Rodrigo et al. (2022) riporta una capacità di adsorbimento aumentata da 9 mg/g a 652 mg/g. Tuttavia, anche in questo caso, la degradazione dei PFAS, indotta dalla magnetizzazione, diviene un potenziale rischio per l’ambiente (Teng et al. 2024).
Trattamento acido-alcalino
Questo tipo di trattamenti del biochar prevedono l’utilizzo di acidi (come l’acido cloridrico, nitrico, citrico o fosforico) per rimuovere la componente cineritica inorganica, aumentare i gruppi funzionali ossigenati, mentre per migliorare la porosità vengono utilizzati l’idrossido di sodio (NaOH) o l’idrossido di potassio (KOH). Questi infatti, agiscono modificando la struttura del biochar aumentandone l’area superficiale, il volume dei pori e l’idrofobicità. Fattori determinanti nei processi fisico-chimici relativi all’adsorbimento dei PFAS49 (Zeng et al., 2021; Zhou et al., 2021).
Anche in questo caso, sebbene siano promettenti, questi trattamenti presentano alcuni svantaggi. I trattamenti acidi, ad esempio, possono causare una grave corrosione delle apparecchiature, sollevando preoccupazioni sui costi operativi e sulla sicurezza. Inoltre, mentre i trattamenti alcalini aumentano l’idrofobicità, possono anche introdurre debolezze strutturali che potrebbero ridurre la longevità del biochar. ed in fine, come nei casi precedenti limitano la sostenibilità del biochar.
Sono in studio anche tecniche di attivazione fisica (SSA e PV), ad esempio, tramite vapore o CO2 (Sørmo et al., 2021). Tuttavia la conclusione rimane la necessità di ulteriori ricerche al fine di rendere questi trattamenti in grado di raggiungere le prestazioni desiderate, ma anche di risultare competitivi nei costi e sicuri per l’ambientale (Nasrollahpour et al., 2025).
| Biochar modificati | PFAS | conclusioni | Contesti | Referenze |
| Biochar-alginate composite beads | PFOS | In meno di 16h è stato ragiunto il tasso di rimozione del 99 %, partendo da una concentrazione iniziale di PFOS di 100 μg L-1 | Soluzione acquosa | (Militao et al., 2023) |
| Biochar rivestito con nanomateriali carboniosi | PFOS, PFOA, | Il biochar rivestito di nanomateriali ha mostrato un tasso di rimozione del 79% per le sostanze PFAS, superando significativamente il tasso di rimozione ottenuto con il trattamento originale del biochar. | Ambiente acquatico | (Patel et al., 2023) |
| PFHxS | ||||
| Biochar modificati termicamente e con ossidi metallici | PFOS | Il massimo adsorbimento di PFOS è stato ragiunto a pH3.1, con valori di 178.1 mg g-1 per I biochar modificati termicamente e 194.6 mg g-1 per I biochar modificati con ossidi metallici. | Soluzione acquosa | (Hassan et al., 2020) |
| Magnetic biochar | PFOS | Il massimo adsorbimento dei PFOS registrato è stato di 120.44 ± 12.37 mg g-1. | Soluzione acquosa | (Hassan et al., 2022) |
| Biochar activated with steam/CO2 | PFOS, PFOA, PFHxS, PFHxA | Il biochar attivato ha mostrato una riduzione significativamente maggiore(63-95%) rispetto al biochar non attivato (23-78%) | Suolo | (Sørmo et al., 2021) |
| FeCl3 and biochar modificato con nanotui di carbonio | PFOA | Il PFOA anionico ha mostrato una maggiore probabilità di aderire alle superfici e di formare legami ionici, determinando così una maggiore capacità di adsorbimento. | Ambiente acquatico simulato | (Wu et al., 2022) |
| Composti di biochar e argille | PFOAB | È stata osservata una significative efficacia per la rimozione dei PFAS zwitterionici. | Soluzione acquosa | (Mukhopadhyay et al., 2021) |
| Tabella 2- Esempi di casi studio di performance adsorbenti di biochar attivati con diverse tecniche. (Liang et al. 2024) | ||||
Costi e disponibilità
Concludendo che le sostanze carboniose, in particolare, il carbone attivo e il biochar riportano delle performance migliori rispetto alle altre proposte. La scelta tra i due è quindi si sposta sul piano economico. Liang et al. (2024) non solo riportano un evidente economicità del biochar rispetto alle altre soluzioni, ma anche in riferimento al carbone attivo, che risulta superare il costo del biochar di circa sei volte (Premarathna et al., 2019). Questo dunque lo rende una valida alternativa al carbone attivo (Alhashimi & Aktas, 2017; O’Connor et al., 2022). Tuttavia, il valore del biochar è fortemente influenzato dalla disponibilità delle risorse (45% sul prezzo finale) (Homagain et al., 2016). Dunque l’economicità del biochar sarebbe da definire localmente. Homagain et al. (2016) però sottolinea anche l’importanza di identificare i metodi di produzione più efficienti ed economicamente sostenibili.
Bibliografia
Askeland, M., Clarke, B.O., Cheema, S.A., Mendez, A., Gasco, G., Paz-Ferreiro, J., 2020. Biochar sorption of PFOS, PFOA, PFHxS and PFHxA in two soils with contrasting texture. Chemosphere 249, 126072. https://doi.org/10.1016/j. chemosphere.2020.126072.
J. Cheng, C.D. Vecitis, H. Park, B.T. Mader, M.R. Hoffmann Sonochemical degradation of perfluorooctane sulfonate (PFOS) and perfluorooctanoate (PFOA) in landfill groundwater: environmental matrix effects Environmental Science & Technology, 42 (21) (2008), pp. 8057-8063
H. Chen, S. Chen, X. Quan, Y. Zhao, H. Zhao. Sorption of perfluorooctane sulfonate (PFOS) on oil and oil-derived black carbon: Influence of solution pH and [Ca2+ Chemosphere, 77 (10) (2009), pp. 1406-1411
X. Chen, X. Xia, X. Wang, J. Qiao, H. Chen A comparative study on sorption of perfluorooctane sulfonate (PFOS) by chars, ash and carbon nanotubes Chemosphere, 83 (10) (2011), pp. 1313-1319
Chen, W., Meng, J., Han, X., Lan, Y., Zhang, W., 2019. Past, present, and future of biochar. Biochar 1, 75–87. https://doi.org/10.1007/s42773-019-00008-3.
Chen, H., Gao, Y., Li, J., Fang, Z., Bolan, N., Bhatnagar, A., Gao, B., Hou, D., Wang, S., Song, H., Yang, X., Shaheen, S.M., Meng, J., Chen, W., Rinklebe, J., Wang, H., 2022. Engineered biochar for environmental decontamination in aquatic and soil systems: a review. Carbon Res. 1, 4. https://doi.org/10.1007/s44246-022-00005-5.
Chen, H., Gao, Y., Fang, Z., Li, J., Pillai, S.C., Song, H., Sun, C., Bolan, N., Yang, X., Vithanage, M., Shan, S., Wang, H., 2024. Investigating the electron-scale adsorption mechanisms using DFT calculations and experimental studies in self-assembly magnetic biochar gel incorporated with graphene nanosheets for enhanced Sb(III) removal. Chem. Eng. J. 150740 https://doi.org/10.1016/j.cej.2024.150740.
Fang, Q., Chen, B., Lin, Y., Guan, Y., 2014. Aromatic and hydrophobic surfaces of woodderived biochar enhance perchlorate adsorption via hydrogen bonding to oxygencontaining organic groups. Environ. Sci. Technol. 48, 279–288. https://doi.org/10.1021/es403711y.
Gagliano, E., Sgroi, M., Falciglia, P.P., Vagliasindi, F.G.A., Roccaro, P., 2020. Removal of poly- and perfluoroalkyl substances (PFAS) from water by adsorption: role of PFAS chain length, effect of organic matter and challenges in adsorbent regeneration. Water Res. 171, 115381 https://doi.org/10.1016/j.watres.2019.115381.
Y. Gao, S. Deng, Z. Du, K. Liu, G. Yu Adsorptive removal of emerging polyfluoroalky substances F-53B and PFOS by anion-exchange resin: A comparative study Journal of Hazardous Materials, 323 (2017), pp. 550-557
Goranov, A.I., Sørmo, E., Hagemann, N., Cornelissen, G., Zimmerman, A.R., Hatcher, P. G., 2024. Using the benzenepolycarboxylic acid (BPCA) method to assess activated biochars and their PFAS sorption abilities. Chemosphere 355, 141750. https://doi.org/10.1016/j.chemosphere.2024.141750.
S.A. Grieco, S. Koenigsberg, J. Claffey, I. Cooper, A. Dewitt, R. Naidu, R. Wymore Ex-situ treatment and residual management of PFAS contaminated environmental media Remediation Journal, 32 (1-2) (2022), pp. 55-6
M. Hassan, J. Du, Y. Liu, R. Naidu, J. Zhang, M.A. Ahsan, F. Qi Magnetic biochar for removal of perfluorooctane sulphonate (PFOS): interfacial interaction and adsorption mechanism Environmental Technology & Innovation, 28 (2022), Article 102593
M. Hassan, Y. Liu, R. Naidu, J. Du, F. Qi Adsorption of Perfluorooctane sulfonate (PFOS) onto metal-oxides modified biochar Environmental Technology & Innovation, 19 (2020), Article 100816
M. Hassan, Y.J. Liu, R. Naidu, S.J. Parikh, J.H. Du, F.J. Qi, I.R. Willett Influences of feedstock sources and pyrolysis temperature on the properties of biochar and functionality as adsorbents: A meta-analysis Science of The Total Environment, 744 (2020)
M. Hassan, R. Naidu, J. Du, Y. Liu, F. Qi. Critical review of magnetic biosorbents: Their preparation, application, and regeneration for wastewater treatment Science of The Total Environment, 702 (2020), Article 134893
M. Hassan, B. Wang, P. Wu, S. Wang Engineered biochar for in-situ and ex-situ remediation of contaminants from soil and water Science of The Total Environment (2024), Article 177384
Hassan M., Naidu R., Qi F., Wang B., Wang L., Asadi S., Deb A. K., Du J., Liu Y. Comparative immobilization of 30 PFAS mixtures onto biochar, clay, nanoparticle, and polymer derived engineered adsorbents: machine learning insights into carbon chain length and removal mechanism. Journal of Hazardous Materials, (2025) doi: https://doi.org/10.1016/j.jhazmat.2025.137742
Karbassiyazdi, E., Kasula, M., Modak, S., Pala, J., Kalantari, M., Altaee, A., Esfahani, M. R., Razmjou, A., 2023. A juxtaposed review on adsorptive removal of PFAS by metalorganic frameworks (MOFs) with carbon-based materials, ion exchange resins, and polymer adsorbents. Chemosphere 311, 136933. https://doi.org/10.1016/j. chemosphere.2022.136933.
Krebsbach, S., He, J., Adhikari, S., Olshansky, Y., Feyzbar, F., Davis, L.C., Oh, T.-S., Wang, D., 2023. Mechanistic understanding of perfluorooctane sulfonate (PFOS) sorption by biochars. Chemosphere 330, 138661. https://doi.org/10.1016/j.chemosphere.2023.138661.
Kundu, S., Patel, S., Halder, P., Patel, T., Hedayati Marzbali, M., Pramanik, B.K., Paz- Ferreiro, J., De Figueiredo, C.C., Bergmann, D., Surapaneni, A., Megharaj, M., Shah, K., 2021. Removal of PFASs from biosolids using a semi-pilot scale pyrolysis reactor and the application of biosolids derived biochar for the removal of PFASs from contaminated water. Environ. Sci.: Water Res. Technol. 7, 638–649. https://doi.org/10.1039/D0EW00763C.
S.P. Lenka, M. Kah, L.P. Padhye A review of the occurrence, transformation, and removal of poly- and perfluoroalkyl substances (PFAS) in wastewater treatment plants Water Research (2021).
Li, J., Gao, Y., Li, C., Wang, F., Chen, H., Yang, X., Jeyakumar, P., Sarkar, B., Luo, Z., Bolan, N., Li, X., Meng, J., Wang, H., 2024a. Pristine and Fe-functionalized biochar for the simultaneous immobilization of arsenic and antimony in a contaminated mining soil. J. Hazard. Mater. 469, 133937 https://doi.org/10.1016/j.jhazmat.2024.133937.
Liang, D.; Li, C.; Chen, H.; Sørmo, E.; Cornelissen, G.; Gao, Y.; Reguyal, F.; Sarmah, A.; Ippolito, J.; Kammann, C.; et al. A critical review of biochar for the remediation of PFAS-contaminated soil and water. Sci. Total Environ. 2024, 951, 174962−174962. https://doi.org/10.1016/j.scitotenv.2024.174962
Lin H., Taniyasu S., Yamazaki E., Wei S., Wang X., Gai N., Kim J.H., Eun H., Lam P.K., Yamashita N. Per-and polyfluoroalkyl substances in the air particles of Asia: levels, seasonality, and size-dependent distribution Environmental Science & Technology, 54 (22) (2020), pp. 14182-14191
Liu, Z., Zhang, P., Wei, Z., Xiao, F., Liu, S., Guo, H., Qu, C., Xiong, J., Sun, H., Tan, W., 2023b. Porous Fe-doped graphitized biochar: an innovative approach for coremoving per-/polyfluoroalkyl substances with different chain lengths from natural waters and wastewater. Chem. Eng. J. 476, 146888 https://doi.org/10.1016/j.cej.2023.146888.
F. Liu, J.J. Pignatello, R. Sun, X. Guan, F. Xiao. A comprehensive review of novel adsorbents for per- and polyfluoroalkyl substances in water ACS ES&T Water, 4 (4) (2024), pp. 1191-1205
Lu, Y., Cai, Y., Zhang, S., Zhuang, L., Hu, B., Wang, S., Chen, J., Wang, X., 2022. Application of biochar-based photocatalysts for adsorption-(photo)degradation/reduction of environmental contaminants: mechanism, challenges and perspective. Biochar 4, 45. https://doi.org/10.1007/s42773-022-00173-y.
Lyu, X., Xiao, F., Shen, C., Chen, J., Park, C.M., Sun, Y., Flury, M., Wang, D., 2022. Perand polyfluoroalkyl substances (PFAS) in subsurface environments: occurrence, fate, transport, and research prospect. Rev. Geophys. 60, e2021RG000765 https://doi.org/10.1029/2021RG000765.
Mayakaduwage, S.; Ekanayake, A.; Kurwadkar, S.; Rajapaksha, A. U.; Vithanage, M. Phytoremediation prospects of per-and polyfluoroalkyl substances: a review. Environ. Res. 2022, 212, 113311.
R. McGregor. In situ treatment of PFAS‐impacted groundwater using colloidal activated carbon Remediation Journal, 28 (3) (2018), pp. 33-41
McMahon P.B., Tokranov A.K., Bexfield L.M., Lindsey B.D., Johnson T.D., Lombard M.A., Watson E. Perfluoroalkyl and polyfluoroalkyl substances in groundwater used as a source of drinking water in the eastern United States Environmental Science & Technology, 56 (4) (2022), pp. 2279-2288
Meng L., Lu Y., Wang Y., Ma X., Li J., Lv J., Wang Y., Jiang G. Occurrence, temporal variation (2010–2018), distribution, and source appointment of per-and polyfluoroalkyl substances (PFAS) in mollusks from the Bohai Sea, China ACS ES&T Water, 2 (1)
Mukhopadhyay, R., Sarkar, B., Palansooriya, K.N., Dar, J.Y., Bolan, N.S., Parikh, S.J., Sonne, C., Ok, Y.S., 2021. Natural and engineered clays and clay minerals for the removal of poly- and perfluoroalkyl substances from water: state-of-the-art and future perspectives. Adv. Colloid Interf. Sci. 297, 102537 https://doi.org/10.1016/j.
R. Naidu, P. Nadebaum, C. Fang, I. Cousins, K. Pennell, J. Conder, C.J. Newell, D. Longpré, S. Warner, N.D. Crosbie, A. Surapaneni, D. Bekele, R. Spiese, T. Bradshaw, D. Slee, Y. Liu, F. Qi, M. Mallavarapu, L. Duan, L. McLeod, M. Bowman, B. Richmond, P. Srivastava, S. Chadalavada, A. Umeh, B. Biswas, A. Barclay, J. Simon, P. Nathanail Per- and poly-fluoroalkyl substances (PFAS): Current status and research needs Environmental Technology & Innovation, 19 (2020), Article 100915.
Nasrollahpour S., Pulicharla R., Brar S. K. Functionalized Biochar for the Removal of Poly- and Perfluoroalkyl Substances in Aqueous Media, ISCIENCE (2025), doi: https://doi.org/10.1016/j.isci.2025.112113.
M.D. Nguyen, A.K. Sivaram, M. Megharaj, L. Webb, S. Adhikari, M. Thomas, A. Surapaneni, E.M. Moon, N.A. Milne. Investigation on removal of perfluorooctanoic acid (PFOA), perfluorooctane sulfonate (PFOS), perfluorohexane sulfonate (PFHxS) using water treatment sludge and biochar Chemosphere, 338 (2023), Article 139412
O’Connor, J., Bolan, N.S., Kumar, M., Nitai, A.S., Ahmed, M.B., Bolan, S.S., Vithanage, M., Rinklebe, J., Mukhopadhyay, R., Srivastava, P., Sarkar, B., Bhatnagar, A., Wang, H., Siddique, K.H.M., Kirkham, M.B., 2022. Distribution, transformation and remediation of poly- and per-fluoroalkyl substances (PFAS) in wastewater sources. Process. Saf. Environ. Prot. 164, 91–108. https://doi.org/10.1016/j.psep.2022.06.002.
Oh, J., Shin, H.M., Kannan, K., Calafat, A.M., Schmidt, R.J., Hertz-Picciotto, I., Bennett, D.H., 2024. oh. Environmental Science & Technology 58(7), 3151-3162
Park, M., Wu, S., Lopez, I.J., Chang, J.Y., Karanfil, T., Snyder, S.A., 2020. Adsorption of perfluoroalkyl substances (PFAS) in groundwater by granular activated carbons: roles of hydrophobicity of PFAS and carbon characteristics. Water Res. 170, 115364 https://doi.org/10.1016/j.watres.2019.115364.
Premarathna, K.S.D., Rajapaksha, A.U., Sarkar, B., Kwon, E.E., Bhatnagar, A., Ok, Y.S., Vithanage, M., 2019. Biochar-based engineered composites for sorptive decontamination of water: a review. Chem. Eng. J. 372, 536–550. https://doi.org/10.1016/j.cej.2019.04.097.
J. Reinikainen, N. Perkola, L. Äystö, J. Sorvari The occurrence, distribution, and risks of PFAS at AFFF-impacted sites in Finland Science of The Total Environment, 829 (2022), Article 154237
Rodrigo, P.M., Navarathna, C., Pham, M.T.H., McClain, S.J., Stokes, S., Zhang, X., Perez, F., Gunatilake, S.R., Karunanayake, A.G., Anderson, R., Thirumalai, R.V.K.G., Mohan, D., Pittman, C.U., Mlsna, T.E., 2022. Batch and fixed bed sorption of low to moderate concentrations of aqueous per- and poly-fluoroalkyl substances (PFAS) on Douglas fir biochar and its Fe3O4 hybrids. Chemosphere 308, 136155. https://doi.org/10.1016/j.chemosphere.2022.136155.
I. Ross, J. McDonough, J. Miles, P. Storch, P. Thelakkat Kochunarayanan, E. Kalve, J. Hurst, S. S. Dasgupta, J. Burdick. A review of emerging technologies for remediation of PFASs Remediation Journal, 28 (2) (2018), pp. 101-126
Saeidi, N., Kopinke, F.-D., Georgi, A., 2020. Understanding the effect of carbon surface chemistry on adsorption of perfluorinated alkyl substances. Chem. Eng. J. 381,122689 https://doi.org/10.1016/j.cej.2019.122689.
J.A. Simon, S. Abrams, T. Bradburne, D. Bryant, M. Burns, D. Cassidy, J. Cherry, S.Y. Chiang, D. Cox, M. Crimi PFAS Experts Symposium: Statements on regulatory policy, chemistry and analytics, toxicology, transport/fate, and remediation for per‐and polyfluoroalkyl substances (PFAS) contamination issues Remediation Journal, 29 (4) (2019), pp. 31-48
Sørmo, E., Castro, G., Hubert, M., Licul-Kucera, V., Quintanilla, M., Asimakopoulos, A.G., Cornelissen, G., Arp, H.P.H., 2023. The decomposition and emission factors of a wide range of PFAS in diverse, contaminated organic waste fractions undergoing dry pyrolysis. J. Hazard. Mater. 454, 131447 https://doi.org/10.1016/j.jhazmat.2023.131447.
Sparrevik, M., Saloranta, T., Cornelissen, G., Eek, E., Fet, A.M., Breedveld, G.D., Linkov, I., 2011. Use of life cycle assessments to evaluate the environmental footprint of contaminated sediment remediation. Environ. Sci. Technol. 45, 4235–4241. https://doi.org/10.1021/es103925u.
Teng B., Zhao Z., Xia L., Wu J., Wang H., 2024. Progress on the removal of PFAS contamination in water by different forms of iron-modified biochar. C h e m o s p h e r e 369 (2024) 143844 https://doi.org/10.1016/j.chemosphere.2024.143844
Thines, K.R., Abdullah, E.C., Mubarak, N.M., and Ruthiraan, M. (2017). Synthesis of magnetic biochar from agricultural waste biomass to enhancing route for waste water and polymer application: A review. Renew. Sustain. Energy Rev. 67, 257–276. https://doi.org/10.1016/J.RSER.2016.09.057.
Z. Wang, A. Alinezhad, R. Sun, F. Xiao, J.J. Pignatello. Pre- and postapplication thermal treatment strategies for sorption enhancement and reactivation of biochars for removal of Per- and Polyfluoroalkyl Substances from water. ACS ES&T Engineering, 3 (2) (2023), pp. 193-200
Van Nguyen, T.T., Phan, A.N., Nguyen, T.-A., Nguyen, T.K., Nguyen, S.T., Pugazhendhi, A., Ky Phuong, H.H., 2022. Valorization of agriculture waste biomass as biochar: as first-rate biosorbent for remediation of contaminated soil. Chemosphere 307, 135834. https://doi.org/10.1016/j.chemosphere.2022.135834.
Wen, C., Liu, T., Wang, D., Wang, Y., Chen, H., Luo, G., Zhou, Z., Li, C., Xu, M., 2023. Biochar as the effective adsorbent to combustion gaseous pollutants: preparation, activation, functionalization and the adsorption mechanisms. Prog. Energy Combust. Sci. 99, 101098 https://doi.org/10.1016/j.pecs.2023.101098.
T. Yan, H. Chen, X. Wang, F. Jiang. Adsorption of perfluorooctane sulfonate (PFOS) on mesoporous carbon nitride. RSC Advances, 3 (44) (2013), pp. 22480-22489
Xing, B., Senesi, N., Huang, P.M. (Eds.), 2011. Biophysico-chemical Processes of Anthropogenic Organic Compounds in Environmental Systems, 1st ed. Wiley. https://doi.org/10.1002/9780470944479.
Xiao, X., Ulrich, B.A., Chen, B., and Higgins, C.P. (2017). Sorption of Polyand Perfluoroalkyl Substances (PFASs) Relevant to Aqueous Film- Forming Foam (AFFF)-Impacted Groundwater by Biochars and Activated Carbon. Environ. Sci. Technol. 51, 6342–6351. https://doi.org/10.1021/ACS.EST.7B00970.
Yang, M., Zhang, X., Yang, Y., Liu, Q., Nghiem, L.D., Guo, W., and Ngo, H.H. (2022). Effective destruction of perfluorooctanoic acid by zero-valent iron laden biochar obtained from carbothermal reduction: Experimental and simulation study. Sci. Total Environ. 805, 150326. https://doi.org/10.1016/J.SCITOTENV.2021.150326.
Zeng, H., Zeng, H., Zhang, H., Shahab, A., Zhang, K., Lu, Y., Nabi, I., Naseem, F., and Ullah, H. (2021). Efficient adsorption of Cr (VI) from aqueous environments by phosphoric acid activated eucalyptus biochar. J. Clean. Prod. 286, 124964. https://doi.org/10.1016/J.JCLEPRO.2020.124964.
Zhang, D., He, Q., Wang, M., Zhang, W., Liang, Y., 2021. Sorption of perfluoroalkylated substances (PFASs) onto granular activated carbon and biochar. Environ. Technol. 42, 1798–1809. https://doi.org/10.1080/09593330.2019.1680744.
D. Zhang, Q. He, M. Wang, W. Zhang, Y. Liang. Sorption of perfluoroalkylated substances (PFASs) onto granular activated carbon and biochar. Environmental Technology (2019).
D. Zhang, Q. He, M. Wang, W. Zhang, Y. Liang. Sorption of perfluoroalkylated substances (PFASs) onto granular activated carbon and biochar. Environmental Technology, 42 (12) (2021), pp. 1798-1809
L. Zhao, Y. Zhang, S. Fang, L. Zhu, Z. Liu. Comparative sorption and desorption behaviors of PFHxS and PFOS on sequentially extracted humic substances. Journal of Environmental Sciences, 26 (12) (2014), pp. 2517-2525
Zhi, Y., Liu, J., 2018. Sorption and desorption of anionic, cationic and zwitterionic polyfluoroalkyl substances by soil organic matter and pyrogenic carbonaceous materials. Chem. Eng. J. 346, 682–691. https://doi.org/10.1016/j.cej.2018.04.042. Zhou, Y., Xu, M., Huang, D., Xu, L., Yu, M., Zhu, Y., et al., 2021. Modulating hierarchically microporous biochar via molten alkali treatment for efficient adsorption removal of perfluorinated carboxylic acids from wastewater. Sci. Total Env
